RNA剪接失调与癌症
前言
RNA剪接失调是几乎所有肿瘤类型的分子特征。癌症相关的剪接改变既来自反复突变,也来自调控剪接催化的反式作用因子的表达改变。癌症相关剪接失调可通过多种机制促进肿瘤发生,导致细胞增殖增加、凋亡减少、迁移和转移潜能增强、对化疗的抵抗和逃避免疫监测。
近年来,对影响癌细胞转化的RNA剪接亚型的深入研究,使我们可以针对这些个体事件开发治疗的新方法。调节或抑制RNA剪接的小分子药物已进入临床开发,成为非常有前景的抗癌药物。
剪接催化与调控
RNA剪接是一个高度调控的过程,由剪接体以及其他调控剪接因子来完成。剪接体识别前mRNA中的核心调控序列,包括标记内含子-外显子边界的5′和3′剪接位点(5′SS和3′SS)、分支点位点(BPS)和多嘧啶区。
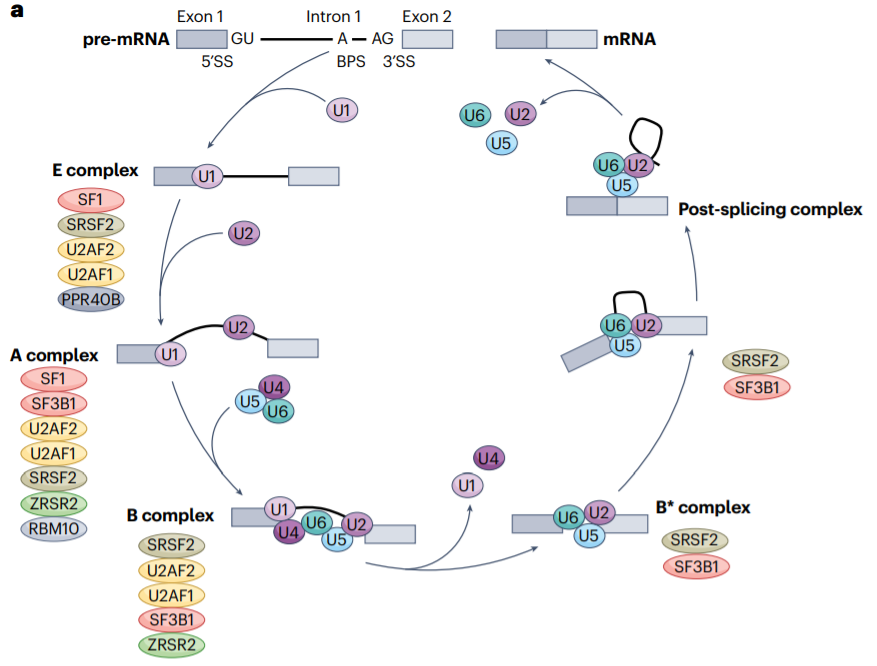
有两种剪接体复合物进行剪接反应,U2型(主要剪接体)或U12型(次要剪接体)。它们主要区别在各自剪接反应中使用的RNA组分以及它们识别的剪接位点序列。U2型剪接体优先识别GT-AG剪接位点,负责去除约99%的内含子;而识别AT-AC和GT-AG位点的U12型剪接体参与去除少于1%的内含子,并调节一组独特的剪接事件。
除了与5′SS和3′SS相邻的核苷酸外,剪接体识别的核心调控序列有很大的多样性。这就需要一个额外的调控,这种调控依赖于顺式作用调控序列和反式作用剪接因子蛋白,可以加强或削弱剪接体对剪接位点的识别。这些顺式作用序列和反式作用剪接因子一起调节选择性剪接,允许单个基因编码多个不同的RNA亚型,这些RNA亚型可以被翻译功能不同的蛋白质亚型。目前估计,每个人类蛋白质编码基因平均编码7.4个RNA亚型。

调节选择性剪接的反式剪接因子是一类RNA结合蛋白(RBPs),它们识别并结合前mRNA上的顺式调节元件,即外显子或内含子剪接增强子(ESE或ISE)或外显子和内含子剪接沉默子(ESS或ISS)序列,并分别促进或抑制该外显子纳入成熟mRNA。
肿瘤发生中的剪接改变
影响剪接机制或剪接因子成分的突变或表达变化可在癌症的发生和发展中发挥关键作用。通过诱导影响许多下游基因的剪接改变,这些改变有可能破坏基因产物和癌症途径的网络。
剪接因子的复发突变
SF3B1、SRSF2、U2AF1和ZRSR2中的复发性体细胞突变经常发生在血液系统恶性肿瘤中,包括骨髓增生异常综合征(MDS)、慢性粒细胞单核细胞白血病(CMML)、急性髓细胞白血病(AML)和慢性淋巴细胞白血病(CLL)。这些突变通常被称为“剪接体突变”。

SF3B1是癌症中最常见的突变剪接体成分,约30%的MDS患者中检测到复发性体细胞突变。SF3B1突变也在其他癌症中检测到,包括15%的CLL、3%的胰腺癌、1.8%的乳腺腺癌、1%的皮肤黑色素瘤和20%的葡萄膜黑色素瘤(UVM)。SF3B1是U2 snRNP的核心成分,参与BPS识别和剪接复合体a组装。SF3B1突变几乎普遍作为杂合错义突变发生,影响羧基末端HEAT结构域(HDs)内的多个热点残基。这些突变导致BPS识别改变,进而导致3′SS识别改变,从而导致广泛的剪接改变。
编码其他剪接体成分的基因也在血液学和实体恶性肿瘤中检测到突变。例如,RBM10在肺癌、甲状腺癌和其他癌症中反复突变,导致剪接断裂和促肿瘤效应。SF3A1、PRPF8、SF1、HNRNPK、U2AF2、SRSF6、SRSF1、SRSF7、TRA2B和SRRM2突变也有报道,尽管发生率相对较低。最近的一项研究表明,超过100个编码剪接体成分的基因包含多种癌症类型的驱动突变。
剪接因子表达改变
剪接因子水平和活性在表观遗传学水平、转录和转录后受到严格控制。调控途径的任何改变都可能导致剪接因子表达的改变,从而导致剪接因子下游靶标的选择性剪接的改变。复发性剪接因子突变在血液学恶性肿瘤中很常见,而剪接因子水平的改变和拷贝数的变化在实体瘤中尤为突出。
剪接因子失调与多种癌症类型之间的因果关系已被确定。值得注意的是,在乳腺肿瘤中上调的几种剪接因子具有致癌功能,足以促进乳腺癌模型中的肿瘤发生。剪接因子也可作为肿瘤抑制剂,因此某些剪接因子下调可有助于肿瘤的发展。
改变剪接因子表达促肿瘤的一个典型例子是乳腺、肺、结肠和膀胱肿瘤中SR蛋白SRSF1的上调。SRSF1过表达增强了与减少细胞死亡、增加细胞增殖和抵抗DNA损伤相关同种型的选择性剪接,导致体内和体外细胞转化。SRSF1可与MYC协同作用,通常导致乳腺癌和肺癌患者的肿瘤分级更高,生存期更短。
在癌症中经常上调的其他剪接因子包括SR蛋白家族的其他成员,例如SRSF4、SRSF6或SR样TRA2β;hnRNP蛋白家族的成员,例如hnRNPA1、hnRNPA2/B1、hnRNPM或PTB;以及其他剪接因子,例如ESPR1、ESPR2、RBM5、RBM6和RBM10。相反,几种剪接因子在人类肿瘤中被下调,包括hnRNPK、ESRP1、ESRP2、RBFOX2、RBM5或QKI。
RNA同种型的异常剪接
肿瘤通常表现出比正常组织更复杂的剪接序列,致瘤性可能与转化过程中出现的癌症特异性替代剪接事件有关。癌症相关的替代剪接亚型可以提供增殖优势,改善细胞迁移和转移,使细胞免于死亡,重新连接细胞代谢或细胞信号,促进有利的微环境,改变免疫反应或实现耐药性。

肿瘤中的差异剪接可导致增加增殖潜能的同种型表达。例如,编码蛋白S6K1的RPS6KB1基因的剪接与持续的细胞增殖和肿瘤生长有关。RPS6KB1-1亚型产生全长蛋白,而通过差异剪接可以产生一个较短的RPS6KB1-2亚型,该亚型缺少一部分激酶结构域并差异激活下游mTORC1信号。RPS6KB1-2在乳腺癌、肺癌细胞和原发性肿瘤中高表达,其敲除降低了癌细胞增殖和肿瘤生长。
为了生存,癌细胞需要获得抵抗细胞死亡的能力。控制细胞死亡的多个基因在剪接水平上受到调节,从而产生不同的亚型,其表现出抗凋亡或促凋亡功能,包括BCL-2家族成员,如BCL2L1、BIM或MCL1。BCL2L1剪接可以产生两种亚型,BCLxL和BCLxS,分别抑制和促进凋亡。
肿瘤抑制因子逃避的一个例子涉及转录因子KLF6,其调节细胞增殖、分化和存活,并且通常通过突变或缺失在肿瘤中失活。KLF6的选择性剪接可以产生致癌亚型KLF6-SV1,而不是全长肿瘤抑制亚型。在前列腺、肺、卵巢、脑、乳腺、胰腺和肝脏肿瘤中检测到KLF6-SV1水平升高,并与生存率低相关。
肿瘤进展中的剪接改变
许多替代剪接亚型与增加的细胞侵袭、血管生成和转移扩散有关。一些编码调节细胞粘附和迁移的蛋白基因在细胞入侵或EMT期间表达不同的剪接同种型。这些包括CD44、RAC1、RON或MENA的选择性剪接,这些剪接可产生使细胞侵袭和转移扩散的同种型。
例如,MENA是调节细胞形态和运动的肌动蛋白成核和聚合调节因子,它产生三种在肿瘤进展中发挥不同作用的主要亚型。包含外显子INV或11a的MENA-INV或MENA11a亚型,以及跳过外显子6产生的MENA?v6亚型。这些剪接事件由许多剪接因子调节,包括ESPR1和ESPR2。在肿瘤进展过程中,它们之间的比例发生变化,MENA-INV和MENA?v6升高,MENA11a降低,并与肿瘤分级和转移相关。
剪接改变还可以影响血管生成,促进肿瘤生长和向远处器官扩散。VEGFA的选择性剪接导致在血管生成中具有不同功能的蛋白质同种型。包含促血管生成的VEGFAxxx亚型和抗血管生成的VEGFAxxxb亚型。两种同种型在体外对其受体表现出相似的亲和力;然而,VEGFAxxxb不能刺激VEGF信号传导,从而抑制血管生成。
此外,选择性剪接还影响免疫细胞发育和功能的多个调节步骤。例如,CD45的选择性剪接是T细胞活化过程中的关键步骤,而CD44选择性剪接参与淋巴细胞活化。类似地,白细胞介素受体的可溶性同种型,如IL-4R、IL-5R和IL-6R,通过免疫细胞中的选择性剪接产生。
剪接改变与耐药性
选择性剪接的改变可通过对靶标或信号转导途径的影响导致对靶向治疗的抵抗。例如,使用vemurafenib(一种BRAF-V600E抑制剂)治疗可选择表达替代剪接BRAF亚型的耐药细胞,该亚型不编码通常调节BRAF二聚和激活的RAS结合域。类似地,BRCA1Δ11q亚型,一种缺少外显子11的变体,促进对聚ADP核糖聚合酶(PARP)抑制和顺铂的抵抗。此外,HER2的选择性剪接,例如跳过外显子16,降低了对HER2靶向抗体trastuzumab的敏感性。

治疗B细胞急性淋巴细胞白血病的一个突破是开发针对CD19的CAR-T细胞疗法。然而,50%的患者由于免疫排斥和T细胞耗竭或靶向表位丢失而复发。表位缺失可由CD19的选择性剪接驱动,产生缺少外显子2且不被CAR-T细胞识别的剪接同种型,导致耐药性。另一个例子是CD22的选择性剪接,外显子5和6的跳过导致对靶向CD22的CAR-T细胞的抵抗。
靶向剪接的癌症治疗
鉴于剪接在肿瘤发生中的关键作用,人们对靶向替代剪接用于癌症治疗有着浓厚的兴趣。各种方法,从抑制关键剪接体蛋白或调控剪接因子到调节特定的选择性剪接事件,都在临床前和临床开发中。

靶向中心剪接体
癌症治疗中靶向剪接的一种方法是抑制剪接体本身。SF3B1是对BPS和3′SS选择至关重要的剪接体组件,限制其功能会在剪接体组装的早期阶段破坏剪接。已经鉴定或开发了多种靶向SF3B1的天然和衍生物分子,包括FR901464及其衍生物;sudemycin E;聚二烯内酯B和FD-895及其衍生物(例如E7107和H3B-8800)。
另一种广谱剪接体抑制剂是异银杏素,它阻止U4/U5/U6三snRNP的募集,并导致剪接体前A复合物的停滞。在临床前模型中,异银杏素治疗影响多种癌症相关途径,包括细胞死亡、侵袭和免疫应答。
靶向替代剪接因子
靶向特异性RBPs和剪接因子的抑制剂开发一直具有挑战性,部分原因是缺乏大多数经典小分子抑制剂方法容易靶向的催化活性位点。最近,通过偶然发现,几种芳基磺胺类药物作为分子胶,通过募集CUL4-DCAF15泛素连接酶复合物导致RBP RBM39降解,RBM39的敲除广泛影响替代剪接事件。目前,芳基磺胺类药物的临床试验正在进行中。
靶向上游调节蛋白
剪接因子受到广泛的翻译后修饰,为治疗干预提供了机会。例如,剪接体蛋白和剪接因子受到广泛的精氨酸甲基化的影响,因此I型(PRMT1、PRMT3、PRMT4、PRMT6和PRMT8)和II型(PRMT5)蛋白精氨酸甲酯转移酶通过Sm蛋白和调控剪接因子的甲基化对组成性剪接和选择性剪接的调控至关重要。已经鉴定出许多抑制I型或II型PRMT的小分子,它们都显示出有前景的临床前活性,其中一些目前处于早期临床试验中。
靶向RNA剪接同种型
由于许多与疾病相关的剪接因子目前不能用小分子药物治疗,因此靶向关键的下游错误剪接RNA可能会提供一种有前途的治疗方法。然而,迄今为止,只有少数通过靶向特定RNA转录物的化合物显示出临床效用。
Risdiplam是美国食品和药物管理局(FDA)批准的第一个用于治疗脊髓性肌萎缩症的小分子,其作用是靶向RNA转录。Risdiplam通过选择性结合SMN2前mRNA中外显子7中的剪接增强子和5′SS下游的内含子来促进外显子7的剪接。
寡核苷酸的剪接调节
剪接切换ASO是一种短的、化学修饰的RNA寡聚体,旨在结合靶标前mRNA中的反向互补序列,从而防止其与剪接机制的相互作用。剪接切换ASO可以设计成专门针对5′SS或3′SS,从而阻止其使用;针对剪接增强子序列,从而防止剪接因子激活剂的结合并促进外显子跳跃;靶向剪接沉默序列,从而防止剪接因子阻遏物的结合并促进外显子的剪接;靶向由于突变而产生的隐性剪接位点,从而恢复野生型剪接位点。
ASO纠正癌症相关的选择性剪接事件已产生细胞系和动物模型中有前景的抗癌表型。例如,BRD9基因编码一个毒性外显子,当发生在SF3B1突变肿瘤中时,该外显子导致其mRNA降解。强制跳过该外显子的ASO可使UVM小鼠模型中BRD9蛋白水平增加,肿瘤体积减少。
靶向替代RNA剪接的新策略
一些旨在靶向剪接因子或特定替代剪接事件的新方法已经出现。一个例子是诱饵寡核苷酸,其通过竞争其天然结合靶点来减弱剪接因子活性。诱饵寡核苷酸诱导类似于靶标剪接因子敲除的转录组变化,SRSF1诱饵可以限制活体中胶质瘤细胞的生长。
另一种方法是使用工程化的U7 snRNA来纠正特定的选择性剪接事件。这种方法改变了U7对组蛋白mRNA加工的特异性,并对其进行重新设计,以阻断特定的前mRNA序列,有效地充当反义分子。这些构建体的稳定表达可以克服传统反义治疗的局限性,因为它们不需要多次给药。到目前为止,这种方法已用于强直性肌营养不良、杜氏肌营养不良症、肌萎缩性侧索硬化症、β-地中海贫血、HIV感染和脊髓肌肉萎缩的模型。
最后,通过基于CRISPR的方法进行基因编辑能够靶向特定的选择性剪接事件。通过基因编辑,人们可以增强或消除感兴趣目标中的特定剪接位点序列,从而促进外显子的剪接或跳过。
小结
过去十年的研究表明,选择性剪接失调不仅是癌症的偶然关联,而是一种几乎普遍存在的基本分子特征,在肿瘤发生和进展中发挥重要作用。因此,对普遍存在的癌症特异性剪接失调的深入研究,将为我们揭示这种剪接失调的机制起源和功能的新见解,并指导我们开发通过调节RNA剪接起作用的新型癌症治疗方法。
参考文献:
1.RNAsplicing dysregulation and the hallmarks of cancer. Nat Rev Cancer.2023Jan 10
原文标题:RNA剪接失调与癌症
-
癌症中的STAT蛋白
2023-01-09 -
癌症中的血液学功能障碍
2023-01-05 -
中核集团首套自主研发的BNCT癌症治疗装备落户山东泰安
2023-01-05 -
癌症靶向治疗的耐药性机制和联合疗法
2022-12-27 -
美国伯克利实验室升级高强度激光系统,可用于癌症放射治疗等研究
2022-12-09 -
设计基于T细胞和NK细胞协同作用的癌症免疫疗法
2022-12-01 -
带你了解癌症治疗靶点:PSMA
2022-11-28 -
从整体免疫肿瘤学的视角看TGF-β对癌症免疫应答的调控
2022-11-24 -
关于mRNA疫苗的一些关键问题
2022-11-18 -
带你认识癌症靶点:MUC1和MUC16
2022-11-15 -
CAR-NK:癌症免疫治疗的新希望
2022-11-14 -
3D生物打印癌症模型:从基础生物学到药物开发
2022-11-09 -
靶向p53癌症治疗药物的研究进展
2022-11-01 -
癌症治疗新的免疫检查点:Siglec受体
2022-10-20 -
相分离会驱动RNA病毒诱导的NLRP6炎性体激活
2022-05-05