药物发现中的斑马鱼疾病模型
前言
斑马鱼(Danio rerio)因其条纹而得名,是一种小型热带鱼,主要生活在南亚地区的河流中。40多年前,斑马鱼作为发育生物学研究的模式生物进入实验室。斑马鱼是实现这一目的的理想选择,因为它们是体外受精的,可以从一对繁殖体中生成数百个胚胎,并且是透明的,能够观察脊椎动物从单个细胞到器官发生的全过程。
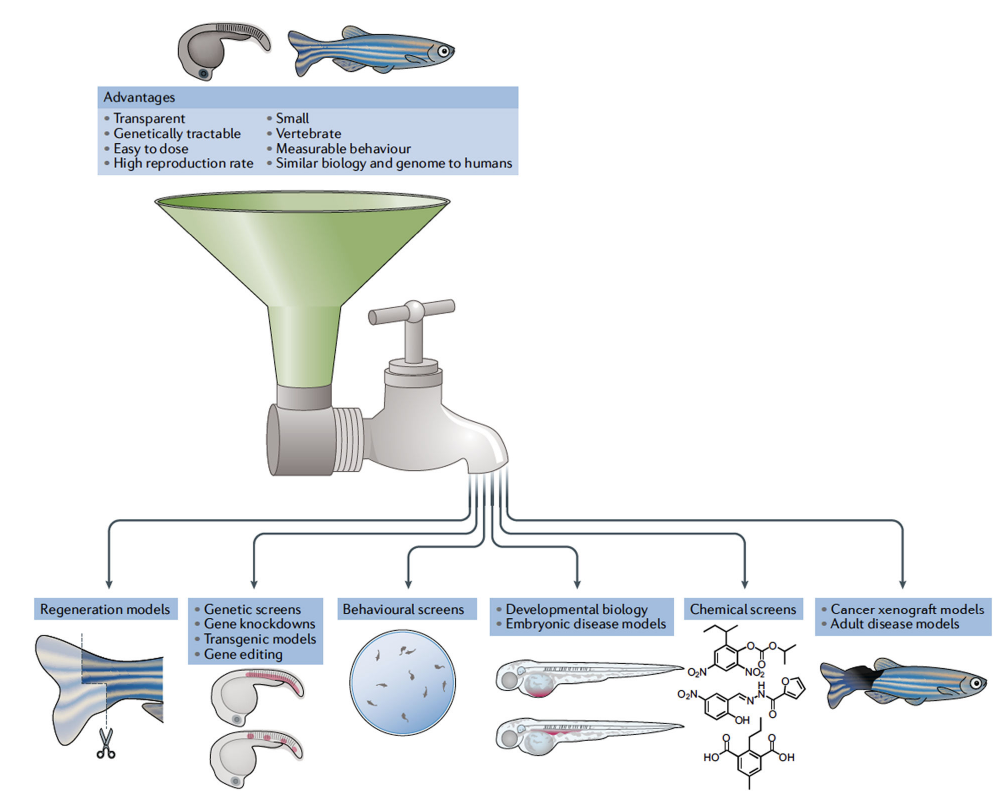
此外,斑马鱼与人类共享70%的基因组,80%以上的疾病蛋白是保守的。至关重要的是,斑马鱼模拟的疾病往往代表了真正的人类疾病模型,现在已成为人类疾病强大的研究工具,斑马鱼模型已广泛用于癌症、肝病、血液病、心脏病和行为障碍等。
斑马鱼表现药物筛选优势
药物发现的一个基本挑战是显示疗效和了解整个活体动物系统内的作用机制。尽管许多化合物和药物先导物在体外或细胞系统中具有活性,但了解药物在器官、组织和身体远端部位的疾病背景下如何发挥作用至关重要。斑马鱼模型在这方面具有独特的优势。
凸显表型特征
斑马鱼是表型药物发现的优良模型系统。在表型药物筛选中,先导药物是根据其产生表型结果的潜力来选择的,与已知和验证的靶点无关。表型药物筛选过程的固有特征包括:即使药物通过靶向多个靶点产生预期的表型结果,例如激酶抑制剂可以通过靶向多个激酶产生治疗益处,也可以识别药物或先导药物;有可能产生广泛的表型结果;针对化合物的反筛选可用于了解其他毒性或不想要的表型。
斑马鱼胚胎的小尺寸意味着可以在活动物中筛选数千个胚胎的表型效应。虽然表型斑马鱼筛选的通量不如细胞培养、酵母、果蝇或体外活性测定中的高,但斑马鱼胚胎的筛选规模超过了目前可用的其他脊椎动物系统。
此外,对于一些药物,斑马鱼比小鼠模型更好地再现了在人类身上看到的效果。沙利度胺就是这种情况。在小鼠中,沙利度胺没有引起任何缺陷;然而,在斑马鱼中,沙利度胺会导致与人类相同的肢体形态缺陷。
体现整合的生理学
斑马鱼几乎具有与人类相同的组织发育和稳态,包括血液、肌肉、心脏、肝脏、胰腺、脾脏、肠道、肾脏、骨骼、脂肪以及神经元和神经嵴的发育。可以筛选药物在组织中的靶向活性,同时提供有关化合物吸收、分布、代谢、排泄和毒性特性的信息。
这种优势提供了有关药物或药物组合常见副作用的重要信息。例如,阿霉素是一种拓扑异构酶II抑制剂,对杀死癌细胞非常有效,但具有心脏毒性和心力衰竭的巨大风险;在用这种药物治疗的斑马鱼身上也观察到了同样的心脏毒性。通过筛选能够预防阿霉素诱导的心肌病的辅助疗法,发现了天然产物visnagin,它可以在不改变阿霉素对癌细胞的细胞毒性的情况下预防心肌病。
最近,这种整合生理学的潜力得到了进一步开发,使用斑马鱼来识别能够抵抗顺铂剂量限制毒性的化合物,顺铂是一种常见的广谱化疗药物,可导致肾损伤和耳聋。通过对肾脏和侧线细胞同时进行毒性筛选试验,发现多巴胺及其相关调节因子具有耳和肾保护作用,而不影响顺铂诱导癌细胞死亡的效力。
筛选试验
斑马鱼筛选试验能够以单细胞分辨率对器官和组织上的药物活性进行深度表型分析。广泛的筛选使用了捕捉发育生物学、细胞增殖、癌症、感染和免疫、行为和毒性等动态的分析。

筛选可以使用抗体(例如磷酸组蛋白H3抗体)在发育中胚胎的单细胞水平上跟踪蛋白质表达,或者固定组织上使用原位杂交跟踪单个细胞中的基因表达。此外,还可以利用斑马鱼从干细胞群中再生组织的显著能力,包括毛细胞、色素细胞、骨骼和脊髓的再生。也可以在药物筛选中使用活胚胎中的荧光报告系统检查单个细胞和组织。例如,使用荧光报告基因筛选胰腺β细胞的调节因子,发现了一组组组蛋白去乙酰化酶(HDAC)抑制剂,即使在高血糖的情况下,也可以降低斑马鱼的血糖水平,并且这些抑制剂在小鼠和人类β细胞模型中具有保守的功能。
斑马鱼模型与人类疾病
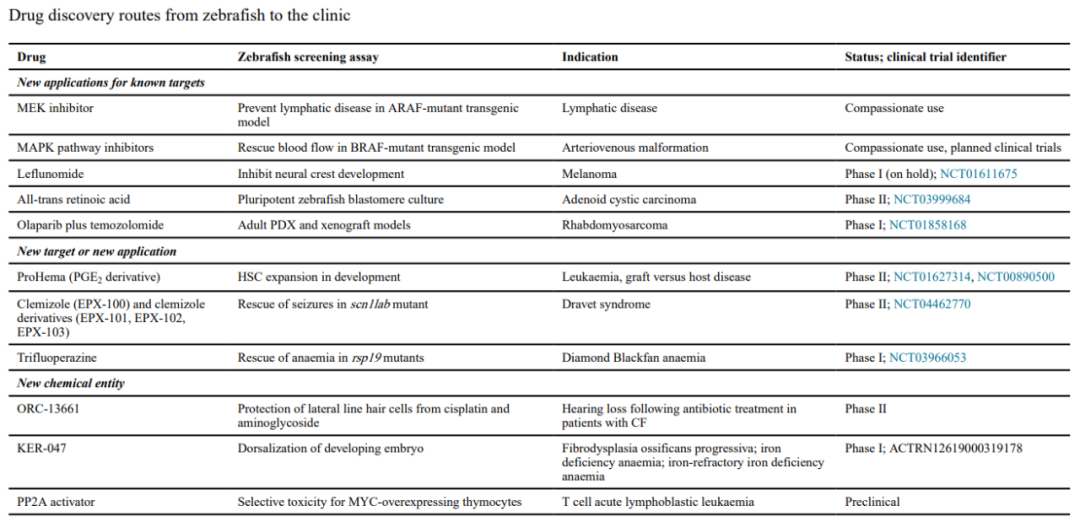
斑马鱼模型为许多人类疾病的基础研究和药物研究提供了重要的见解,许多被发现在斑马鱼体内具有拯救疾病活性的小分子已经进入临床试验。
耳毒性
与耳聋相关的先天性Usher综合征已使用斑马鱼精确建模。斑马鱼侧线毛细胞与哺乳动物内耳毛细胞的功能相似,已用于筛选预防氨基糖苷类抗生素的耳毒性药物。ORC-13661是通过斑马鱼模型筛选出的先导药物,ORC-13661通过高亲和力阻断外毛细胞中的机械电传导通道,从而保护毛细胞免受氨基糖苷类药物和顺铂诱导的耳毒性。
ORC-13661的第一阶段双盲安慰剂对照研究于2019年完成,其耐受性良好。与安慰剂组相比,无严重的治疗相关的不良反应,效力呈现剂量相关性。基于这些结果,不久将开始一项二期研究,以评估ORC-13661是否可以保护囊性纤维化患者的听力损失。另一组可能受益于ORC-13661的患者是非结核分枝杆菌感染患者,他们经常使用氨基糖苷类抗生素治疗,这可能会导致听力损失。
干细胞移植
在斑马鱼发育中的主动脉中寻找造血干细胞诱导物的化学筛选表明,PGE2可以直接刺激造血干细胞的产生和植入。这一原理也在小鼠骨髓移植中得到了证实。
随后在一期临床试验中测试了PGE2,在该试验中,白血病患者接受两个脐带血单位作为干细胞的替代来源,一个用dmPGE2处理,另一个未经处理。两者都被移植到患者体内,白细胞中的DNA多态性显示,12名患者中有10名接受dmPGE2治疗的脐血中的中性粒细胞和血小板优先植入,接受dmPGE2治疗的患者血液植入增强,并且随后没有发生移植物抗宿主病。目前,这种治疗方法已成为基因治疗试验中处理造血干细胞的常用方法,它可以改善病毒转导和干细胞效应。
遗传性癫痫
Dravet综合征是一种由SCN1A突变引起的儿童难治性癫痫性脑病。与许多遗传形式的癫痫一样,Dravet综合征没有明确或令人信服的治疗方法。scn1lab功能缺失突变的斑马鱼具有自发的电图癫痫发作和痉挛样游泳行为,具有儿童Dravet综合征的临床特征。此外,与患者一样,斑马鱼Dravet综合征模型对抗癫痫药物具有抗药性。
通过对3000多种市售和FDA批准的药物进行筛选,发现5-HT受体激动剂clemizole是scn1lab突变体中自发癫痫发作的化学抑制剂,可抑制痉挛样行为。EpyGenix Therapeutics目前正在开发用于临床的clemizole(EPX-100)和clemizole衍生物(EPX-101、EPX-102和EPX-103)。一期研究证实,EPX-100是安全的,儿童耐受性良好,EPX-100现已进入二期临床试验,2020年11月首次给药。
黑色素瘤
斑马鱼黑色素瘤模型对于理解该疾病的基因组学和病因学以及识别新的治疗策略至关重要。斑马鱼黑色素瘤与人类黑色素瘤具有相同的分子和组织病理学特征,表明这些模型与黑色素瘤癌症生物学和药物发现相关。
黑色素瘤起源于黑素细胞谱系,即在发育过程中从神经嵴出现的色素细胞。通过斑马鱼神经嵴上的小分子筛选,天然化合物咖啡酸苯乙酯(CAPE)被证明是调节神经嵴的新型调节剂;此外,抗真菌的clotrimazole被证明在KIT转基因斑马鱼模型中抑制异位黑色素细胞,并在黑色素瘤细胞中具有活性。
腺样囊性癌
腺样囊性癌(ACC)是一种罕见的恶性头颈癌,起源于唾液腺。复发或转移性ACC没有标准的治疗手段,大多数患者在诊断后2年内死亡。大多数ACC具有复发性MYB易位,ACC在分子水平上的特征是主转录因子MYB及其控制增殖和分化的靶基因的过度表达。
目前很少有实验模型可用,培养原代ACC细胞一直是一个挑战。通过使用斑马鱼细菌人工染色体(BAC)报告系统,能够高通量筛选myb-GFP表达细胞的调节因子。通过重复筛选3840个生物活性小分子,发现全反式维甲酸(ATRA)对myb–GFP表达具有有效和选择性的抑制作用。目前,一项机构发起的全反式维甲酸二期研究正在进行中(NCT03999684),尽管完整的试验结果尚待确定,但在2021美国癌症研究协会年会上提交的早期报告表明,某些患者总体耐受性良好,具有一定的稳定作用。
未来方向和展望
药物发现仍然是一个昂贵而费力的过程,实验室和临床环境之间的巨大科学鸿沟阻碍了药物开发。考虑到斑马鱼和人类之间的共同药物反应,斑马鱼可能与哺乳动物模型一样具有强大的临床前预测效果。
斑马鱼和人类之间共有的生理学特征使斑马鱼成为药物开发的重要工具,为新药物类别打开了大门。斑马鱼正在成为人类癌症的化身,未来的研究可能进一步涉及其他组织和器官之间的跨物种异种移植,用于药物研究。为了更好地将新的药物使用从斑马鱼转化到人类,需要进一步努力了解斑马鱼体内的药代动力学。
展望未来的斑马鱼药物筛选,将多个筛选参数纳入整个动物筛选将有助于我们了解化学靶点和药物治疗的反应,包括远端靶点和非靶点药物作用。单细胞组学技术将能够在大细胞群体中评估药物的影响,提供疾病的细胞表现以及如何解决疾病的前所未有的细节。目前,斑马鱼疾病模型和小分子筛选已经展示出令人激动的结果,这也将使斑马鱼为未来的人类疾病治疗做出更重大的贡献。

原文标题:药物发现中的斑马鱼疾病模型
-
Meta免费开源AI模型NLLB-200!可精准翻译超过200种语言
2022-07-08 -
中国电科院研发变电模型转换工具实现自动化系统模型向信息化系统模型的自动转换
2022-07-06 -
世界一流财务 | 全面预算管理帮助集团企业构建7大核心能力
2022-06-28 -
ADC药物的免疫原性
2022-06-20 -
从科研创新到产业落地 华为发布人工智能大模型全流程使能体系
2022-06-15 -
吃药也可“编程”?盘点全球11家3D打印药物企业
2022-05-13 -
从类器官到类器官芯片,药物研发需要新方法
2022-05-10 -
开启未来之窗:AI与药物研发的共舞
2022-05-10 -
自然语言处理序列模型——HMM隐马尔可夫模型
2022-04-13 -
4种在生产中扰乱计算机视觉模型的方法
2022-04-06 -
国网新疆电力开发应用智能分类程序
2022-03-30 -
又一款15MW漂浮式海上风电基础上线在即!
2022-03-30 -
西北电网调控云新能源模型管理平台正式上线运行
2022-03-21 -
FORESEE参数模型提取设计仿真
2022-03-15 -
精彩论文 | 火电机组一次调频功率响应特性精细化建模
2022-03-09